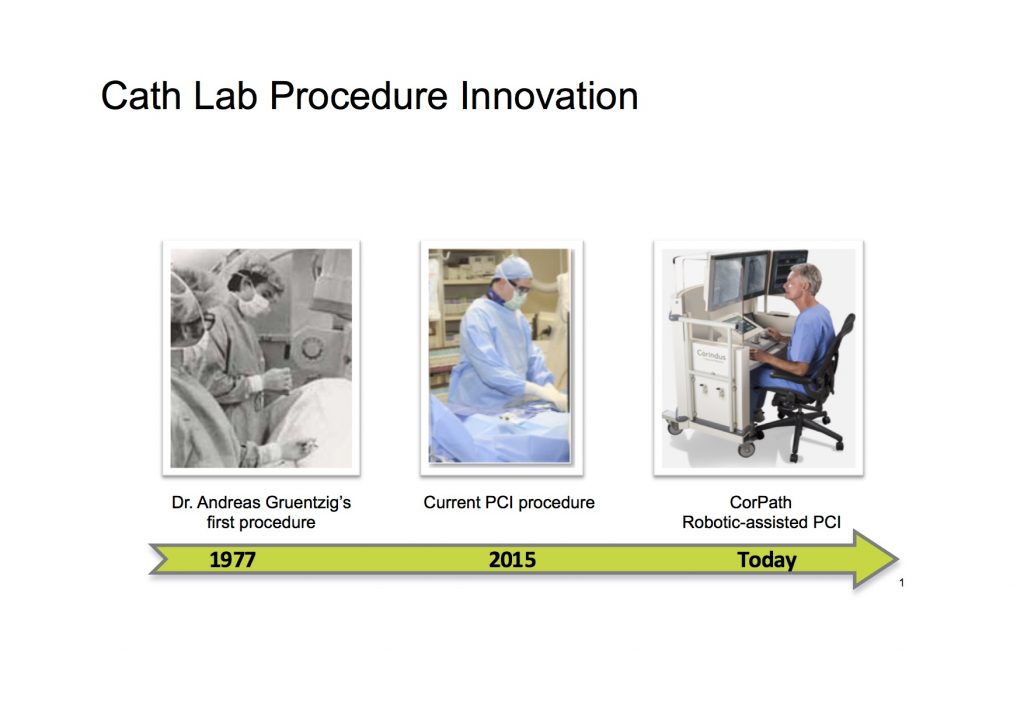
40年前、胸を切らないで冠動脈を治療したいと描いたGruentzigの夢は、デバイスの進化により冠動脈の局所治療としては現実のものとなり、冠動脈インターベンション(PCI)は冠動脈疾患治療の中心的な役割を担っている。
このPCIのイノベーションはバルーンから、ステント、薬剤溶出性ステント(DES)と冠動脈を拡張するデバイスのプロダクト・イノベーションにより達成されてきたが、PCI術者の視点からは、放射線管球の近くに立ち、手動でガイドワイアー(GW)を操作し、バルーン(BA)を挿入し、ステント(ST)を植え込む手技はPCI第一例目と、ほとんど変わっていないのが現状である(図1)。
現在、初期のPCIに比較してより複雑な病変に治療するが故に、手技時間は増加し術者の放射線被曝料は増加している。
心カテ室内で働く我々PCI術者は自らを守るために重い鉛入りのプロテクターを身にまとい、甲状腺や目を守るためにプロテクターを装着しPCIを行ってきた。
しかし近年、低用量放射線被爆による認知症1)や甲状腺癌2)に加えて、PCI医は白内障を放射線量依存性に罹患すること3)、脳腫瘍が左側に発生しやすいこと4)が報告されている。
また、症例数が多い術者ほど整形外科的疾患に罹患しやすいことも報告されている5)。
このような問題を解決するために、PCIの領域にも手術用ロボット技術の導入が検討されるようになった。
本稿では、本邦に導入が予定されている、2012年7月にFDAがPCI補助ロボットとして承認したCorindus社のCorindus Vascular Robotics (CorPath200、CorPath GRXシステム)について解説する。
1. CorPath200 System
CorPath200 System(CorPath)はイスラエル出身の循環器内科医ラファエル・ビザー氏によって開発され、Corindus社が製品化したものである。
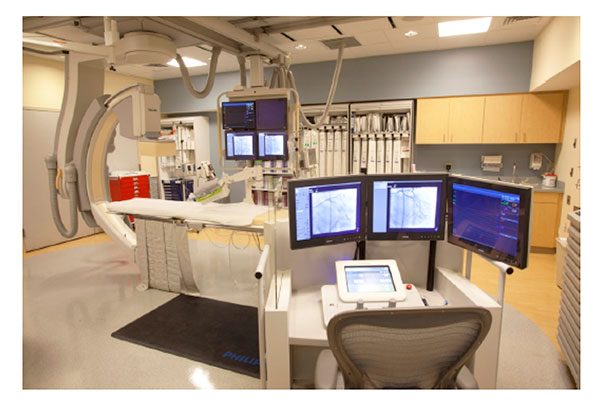
PCI術者はCorPath(図2)を使用することにより、放射線から離れた場所に座りながら、冠動脈に通したGW,BA,STを遠隔的にアクセス、操作が可能である。
PCI術者は独立したX線透視法で直感的なコントロール機能を利用してインターベンション装置を操作する。
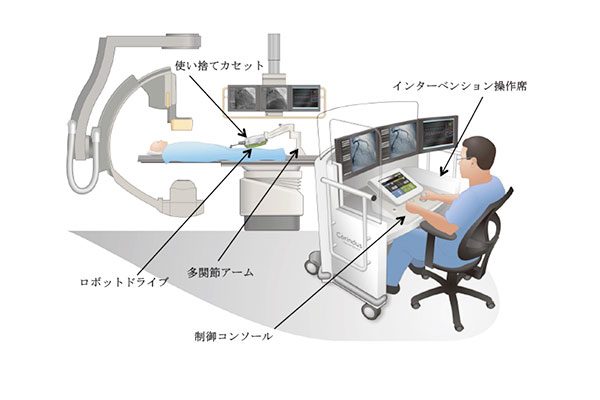
CorPathは図3で示すように、ベットサイドユニットとリモートワークプレースと呼ぶ2つの機能サブユニットから構成される。
ベットサイドユニットは多関節アーム、ロボットドライブ、使い捨てカセットから構成される。
リモートワークプレースは制御コンソールを含むインターベンション操作席(放射線防護付き)、血管造影モニター、血行動態モニター、X線フットペダルから構成される。
GW、BA、STは使い捨てカセットに取り付け、PCI医はジョイスティックまたは制御コンソールのタッチスクリーンを使用することで、GWを進め、抜き、回転させ、BA、STを進める、抜くなどの指示をロボットライブに送信できる。
2. CorPathによるRobotic PCIの臨床試験
CorPathはベンチテストによる非臨床試験、動物での性能試験、生体適合性試験などを経て、2010年にFIM試験(CORBIC試験)が行われた。
本試験はコロンビアのCORBIC Centerで8名の被験者を対象に実施された。
試験の目的はPCIで使用される市販のGW、BA、STのアクセスと操作におけるCorPathの安全性と技術的有効性を明らかにするために施行された。
全ての症例に有害事象を認めることなくCorPathによるRobotic PCIは成功した6)。
CORBIC試験の良好な成績を踏まえて、一枝病変に対するCorPathを用いたRobotic PCIの有効性と安全性を明らかにするため、9施設で164名の冠動脈疾患患者を対象にPRECISE試験が施行された。
57%が不安定狭心症であったが、対象病変は病変長24mm未満の新規病変で、複雑病変は除外された。
臨床的治療成功は97.6%、機器の技術的成功は98.8%に得られ、試験前に規定した臨床評価指標を上回るものであった。
副次評価項目として評価した操作席での照射線量は治療台での照射線量と比較して95.2%有意に減少した(P<0.0001)。
PRECISE試験の結果よりCorPathを用いたRobotic PCIの有効性と安全性が明らかとなった7)。
PCI術者の被曝量低減効果を明らかとするために、STEMI患者、ショック患者、3つ以上の病変を有する患者を除外した連続30例を手動によるPCIとCorPathを用いたRobotic PCIを無作為に比較する試験が施行された。
カテ室内の検査助手の放射線被曝量はRobotic PCI群でやや低下し、医師の放射線被曝量はRobotic PCI群で0.8μSv、手動PCI群で9.1μSvと有意に低下した(P=0.015)。
PRECISE試験に登録したRobotic PCI 40例と手動PCI80例を比較した単施設比較試験においてはRobotic PCI群で透視時間が17%減り、患者被曝量も18%低下した8)。
複雑病変に対するCorPathを用いたPCIの有効性と安全性を明らかとするために、手動PCIと比較したCORA-PCI試験9)が行われた。
108例のRobotic PCIと226例の手動PCIが施行され、対象病変はB2/C病変がRobotic PCI群で81%、手動PCI群で69%であった。
Robotic PCI群の成功率は手技成功92%、臨床的成功99%で、手技時間は手動PCI群と同等であった。
実臨床においてCorPathを用いたRobotic PCIの有効性と安全性を明らかとするために、前向きPRECISIONレジストリ試験10)が行われている。
754人の冠動脈疾患患者を対象に949病変に対してCorPathによるRobotic PCIが施行された。
ACC/AHAクラスB2,C病変が63%含まれていたが、橈骨動脈アプローチが60%に施行され、臨床的成功は大腿動脈アプローチ94.9%、橈骨動脈アプローチ98.9%と高率であった。
手動PCIへの切り替えは両アプローチとも12%で、複雑病変に対しても、アプローチの部位に関わらずCorPathを用いたRonotic PCIの有効性と安全性が明らかとなった。
3. Robotic PCIへの期待
これまで施行された臨床試験よりCorPathを用いたRobotic PCIは単純病変のみならず複雑病変に対しても、術者の被曝量のみならず患者の被曝量を低減し、従来の手動PCIと同等の有効性と安全性で手技が施行できることが明らかとなった。
しかし、PRECISIONレジストリ試験において手動PCIへの切り替えが12%に施行されており、Robotic PCIで完結は得られていなし。
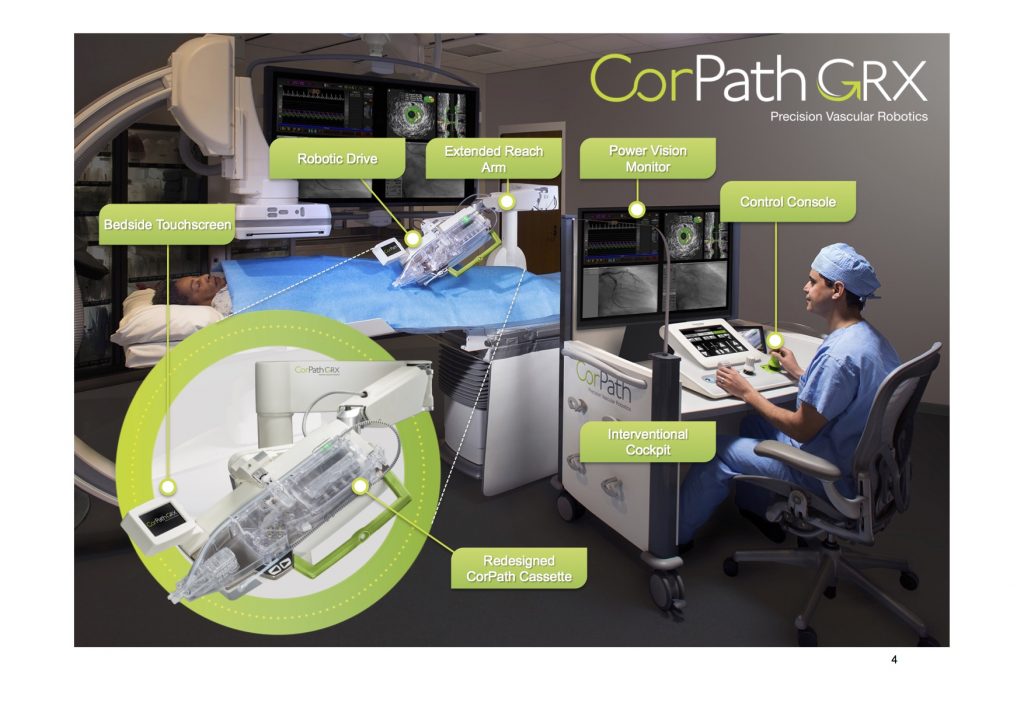
そこで、CorPath200 SystemからCorPath GRX System(図4)へのシステム改良が行われ、既にFDAの承認を取得している。
CorPath200 Systemの機能に加えてガイドカテ(GC)をリモートワークプレースからジョイスティックで操作可能となり、手動操作を加えずとも適切なGCのバックアップサポートを得ることが可能となり、BAやSTの複雑病変への挿入も容易となり、成功率の向上が期待される。
被爆低減のみならずRobotic PCIが患者アウトカム改善に貢献する可能性が示唆されている。
DESの再狭窄は病変に対して不適切な位置に植え込むことにより生じることが知られており、STLLR試験11)ではDES植え込み手技の66.5%に不適切な植え込みが生じ、病変部に起因する心筋梗塞や再血行再建術が高率に発症することが報告されている。
手動PCIで行う視覚的評価では35%しか正確な病変長を評価することは出来ず、Robotic PCIではCorPathによる正確な病変長の評価が有効であることが報告されている。
Robotic PCIを施行したPRECISE試験(n=164)と手動PCIを施行したSTLLR試験(n=1509)の比較では病変に対する不適切なステント植え込みは、手動PCI群43.1%、Robotic PCI群12.2%で有意に低率であった(P<0.0001) 12)。
Propensity sore matchさせた39例では病変に対する不適切なステント植え込みは手動PCI群64.1%、Robotic PCI群10.3%で有意に低率であった(P<0.0001)。
この違いは単に正確な病変長評価のみならず、Robotic PCIにおいては座位で大きなスクリーンを見ながら手技が可能で、術者の疲労は少なく、昼夜間帯における手技のばらつきが少ないことも要因と思われる。
この他にも、GWが固定されているのでデバイス挿入時にGWが前方に進むことはなく、手動PCIで稀に生じるGWによる穿孔が皆無となることが予測される。
GWの操作感は手動PCI とは異なり、病変通過時の感覚的情報はRobotic PCIでは得られないため、GW操作においてやや困難さがあるかもしれないが、手動PCIに比べてGWを点ではなく線で固定しているため、トルク性はより伝わりやすく、操作性に優れる可能性も期待される。
今後の機器の改良で先端にセンサーを付けプラーク情報を集めるGWが開発されれば、経験が重要となる完全閉塞病変に対するPCIにおいて手動PCIよりも順行性で高い成功率を得ることができるかもしれない。
ダビンチ手術時の糸縫合の感覚は手動とは異なり、画像を通じて、繰り返すトレーニングにより習得したと本邦におけるRobotic心臓手術の第一人者である渡辺剛医師は語っており、Robotic PCIも同様なのかもしれない。
冠動脈のみならず末梢血管へもRoboticを用いたインターベンションの適応は拡大している。
RAPID試験では20例の下肢閉塞性動脈硬化症患者(跛行患者90%)の29病変にRobotic 血管内治療を行い、全例に成功した。
今後、頸動脈、頭蓋内動脈インターベンションなど様々な血管領域への適応拡大も期待される。
参考文献
1. D. Marazzitti. Current Medical Chemistry, 19:1864-1869 (2012).
2. E. Ron et al. Radiation Research, 174:877-888 (2010).
3. E. Vano, et al. Journal of Vascular Interventional Radiology 2:197-204(2013).
4. A. Roguin, et al. American Journal of Cardiology 9:1368-72 (May 2013).
5. Catheter Cardiovasc Interv. 2015 Nov;86(5):913-24.
6. Granada J , et al: Journal of Ameican College of Cardiology Intervention 2011; 4; 460-465
7. Weisz G et al; Journal of Ameican College of Cardiology 2013; 61: 1596-600
8. Smilowitz et al, J Invasive Cardiol, 2014;26(7):318-321.
9. Mahmud E. et al. Presented at SCAI 2016.
10. Mahmud E. et al. Presented at SCAI 2017.
11. Costa MA, et al; Am J Cardiol. 2008 Jun 15;101(12):1704-11.
12. Bezerra HG, et al: J Interv Cardiol. 2015 Oct;28(5):449-55.